- 铼的性质及化合物
- 物理性质
- 铼为银白色金属或灰到黑色粉末;熔点3186℃,沸点5596℃,密度为20.53g/cm³。金属铼非常硬,耐磨,耐腐蚀。
- 化学性质
- 铼的电子构型为[Xe]4f145d56s2,氧化态有0、-1、+1、+2、+3、+4、+5、+6、+7,主要氧化态为+3、+4、+5、+7。铼的化学活泼性取决于他的聚集态,粉末状金属铼活泼。铼不溶于盐酸,溶于硝酸,生成高铼酸:3Re+7HNO3→3HReO4+7NO+2H2O。它也溶于含氨的过氧化氢溶液中,生成高铼酸铵:2Re+2NH3+4H2O2→2NH4ReO4+3H2
- 铼氧化物
- 七氧化二铼(Re2O7):黄色固体,具有挥发性,最常见的氧化铼。溶于水,形成高铼酸HReO4。
- 二氧化铼(ReO2):深褐色固体物质。单斜晶结构。密度11.4~11.6g/cm³。沸点1363℃。但700℃开始分解,生成金属铼和七氧化铼。具有吸气性能,挥发性比较差,在空气中与碱共熔可形成高铼酸盐。稍溶于水,不溶于稀酸,可溶于浓的卤族酸中。易与硝酸、过氧化氢等作用生成铼酸。制取方法在300℃下用氢还原铼酸酐,或400℃在惰性介质中(氩、氮)中使铼酸铵分解。为氢还原制取金属铼原料和有机化合物合成催化剂。
- 三氧化铼 (ReO3):红色,不溶于水。
- 三氧化二铼 (Re2O3)
- 氧化二铼(Re2O)
- 五氧化二铼(Re2O5)
- 其他铼化合物
- 铼与硫蒸气在高温下化合生成二硫化铼。
- 铼与硼的化合物二硼化铼(ReB2),硬度极高,与碳化钨、碳化硅、二硼化钛和二硼化锆相近。
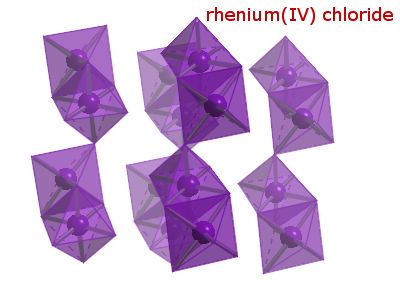 铼与卤素中的氟、氯和溴反应生成卤化物,如四氟化铼 ReF4、五氟化铼ReF5、六氟化铼ReF6、七氟化铼ReF7、五氯化铼ReCl5、六氯化铼ReCl6、三氯化铼ReCl3等。铼的卤化物和卤氧化物均易水解。ReCl3是三聚红色固体,为共价化合物,在溶液中是非电解质。四价铼能形成多种配位化合物。
铼与卤素中的氟、氯和溴反应生成卤化物,如四氟化铼 ReF4、五氟化铼ReF5、六氟化铼ReF6、七氟化铼ReF7、五氯化铼ReCl5、六氯化铼ReCl6、三氯化铼ReCl3等。铼的卤化物和卤氧化物均易水解。ReCl3是三聚红色固体,为共价化合物,在溶液中是非电解质。四价铼能形成多种配位化合物。- 铼还能形成羰基化合物Re(CO)5和高铼酸盐M3ReO5(M为一价金属),锰和锝都没有类似的盐生成。
- 目录
Rhenium
- 介绍
- 历史及发展
- 性质
- 分布产量
- 应用
- 冶炼工艺
- 回收利用
- 行业政策
- 名企
- 推荐
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- 涨 • 知识
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
1 氢 |
2 氦 |
||||||||||||||||||||||||||||||
3 |
4 铍 |
5 硼 |
6 碳 |
7 氮 |
8 氧 |
9 氟 |
10 氖 |
||||||||||||||||||||||||
11 钠 |
12 |
13 |
14 |
15 磷 |
16 硫 |
17 氯 |
18 氩 |
||||||||||||||||||||||||
19 钾 |
20 |
21 |
22 |
23 |
24 |
25 |
26 铁 |
27 |
28 |
29 |
30 |
31 |
32 |
33 |
34 |
35 溴 |
36 氪 |
||||||||||||||
37 铷 |
38 |
39 |
40 |
41 |
42 |
43 锝 |
44 钌 |
45 铑 |
46 钯 |
47 银 |
48 |
49 |
50 |
51 |
52 |
53 碘 |
54 氙 |
||||||||||||||
55 铯 |
56 钡 |
57 |
58 |
59 |
60 |
61 |
62 |
63 |
64 |
65 |
66 |
67 |
68 |
69 |
70 |
71 |
72 铪 |
73 |
74 |
75 |
76 锇 |
77 铱 |
78 铂 |
79 金 |
80 |
81 铊 |
82 |
83 |
84 钋 |
85 砹 |
86 氡 |
87 钫 |
88 镭 |
89 锕 |
90 钍 |
91 镤 |
92 铀 |
93 镎 |
94 钚 |
95 镅 |
96 锔 |
97 锫 |
98 锎 |
99 锿 |
100 镄 |
101 钔 |
102 锘 |
103 铹 |
104 鑪 |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 鐽 |
111 錀 |
112 Cn |
113 Uut |
114 Fl |
115 Uup |
116 Lv |
117 Uus |
118 Uuo |



